張金堅:不要輕忽晝夜節律,與癌症的發生亦有關係
1-1.jpg
本文摘自<常春月刊>476期
文:張金堅(乳癌防治基金會董事長)
由於從簡單的細菌到複雜的靈長類(包括人類),甚至植物,都有「晝夜節律」(circadian rhythm),又叫「約日節律」或「日變節律」,另外亦較常聽到的所謂「生理時鐘」(biologic clock)。在生醫學界中,通常以晝夜節律來描述一日之週期變化。Circa在拉丁的字首代表著「大約」、「大概」的意思,而diem(dian)在拉丁文的定義則是「一天」的意思,地球上的生物為什麼會出現晝夜節律現象呢?
基本而言,此等晝夜節律幫助地球上所有生物為白天的陽光和高溫,以及夜晚的黑暗和寒冷做好準備。好像含羞草白天張開葉子接受第一道陽光進行光合作用,晚上合起葉片一樣;羚羊在晨昏時出現在河邊,獅子就會在晨昏時前往水邊獲取獵物;在較於寒冷高緯度的動物需要在日落前找好棲身之地,才能躲過夜晚的寒冷。
這些案例證明了晝夜節律(生理時鐘)有其需要及功能存在,就好像正常人在一天24小時當中,因應日照、睡眠、休息、飲食、運動,其血壓、體溫及各類荷爾蒙也有週期性的起伏(圖一)。總之,從簡單的細菌、果蠅到複雜的靈長類,為什麼會有如此規則的節律呢?本文將由神經解剖及基因調控兩大方面來探討。

有關晝夜節律在神經解剖方面的相關探討
在1960年代,德國生理學家艾許夫博士(Jurgen Aschoff)將數名受試者個別關在沒有自然光的倉庫裡,發現即使在這樣的環境中,受試者仍保有大約24小時的睡醒週期(sleep-wake cycle),後來哈佛大學的柴斯勒(Chales Czeisler)及克諾勞爾(Richard E Kronauer)也發現同樣的現象。可見受試者的生理現象,並未受到人造環境的影響,不管是體溫、血壓或血液內各類激素濃度的變化,仍遵循24小時的規律。
直到1972年,芝加哥大學的摩爾博士(Robert Moore)及加州大學柏克萊分校的朱克教授(Irving Zucker)終於藉由腦損傷研究證實:人體體內的確有自行運作的生理時鐘,並證實調控晝夜節律的關鍵腦區就是在大腦下視丘(hypothalamus)中的視叉上核(suprachiasmatic nucleus,SCN),如SCN損傷,則無法表現正常的晝夜節律,在小鼠的試驗亦得到證實。
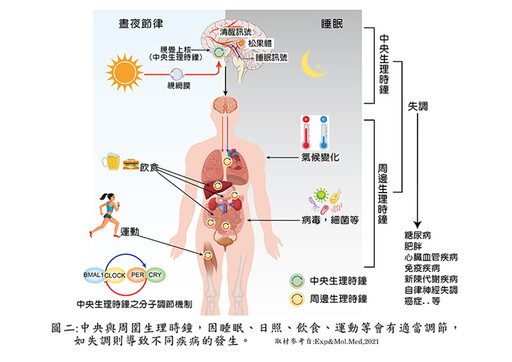
一般而言,當外界光線刺激可經由視神經,再經視網膜下視丘腦管道(retinohypothalamic tract, RHT)傳達到視叉上核(SCN),再影響到與晝夜節律有關的腦區,例如分泌褪黑激素的松果體(Pineal body),而後會有一系列的連續反應,因此視叉上核(SCN)被認為是最重要的中央生理時鐘,它主宰晝夜節律,會影響身體所有的器官、組織(如肝臟、胰臟、心臟、肺臟、血管、腎臟、淋巴系統及內分泌系統)等周邊的區域性生理時鐘,這些區域性的生理時鐘也會因為環境或各項生活因素,如天氣溫差變化、飲食、活動或休息等因素因應產生變化,並與中央生理時間同步協調(Synchronization),藉此調節各項生理功能,使身體維持在最佳的健康狀態。
如果熬夜、不規律生活、睡前大量攝食、沒有定期適當運動、長期夜班工作或飛行造成時差,都會使生理時鐘紊亂、交感神經活性上升、腎上腺素增加、胰島素阻抗性增加、導致血壓及血糖上升,同時有10種以上與發炎有關的介白素產生,免疫功能低下,易患心血管疾病、糖尿病,新陳代謝功能亦受影響,可能造成病態性肥胖,另外與精神有關的毛病,如:焦慮、憂鬱等,甚至造成記憶力減退,注意力不集中、失智等,最近研究發現與癌症亦有關聯(圖二)。
有關晝夜節律在分子控制方面的相關探討 有關於晝夜節律分子機制及基因研究,始自果蠅,由於果蠅體型小、生命週期短、繁殖快速,是進行此類研究的極佳模型,在1970年代,加州理工學院的科諾卡(Ron Konopka)和班瑟(Seymour Benzer)進行果蠅研究,利用誘變劑(mutagen),使果蠅發生基因突變,結果有兩種突變,一種小於正常24小時的短週期(19小時),及另一種大於24小時(28小時)的突變,後來由洛克斐勒大學的楊恩、布倫戴斯大學的霍爾(Jeffery Hall)和霍華休斯醫學中心的羅斯巴希(Michael Rosbash)相繼展開研究。
結果在1980年由楊恩及其團隊發現在X染色體有一基因突變命名為PERIOD(簡稱PER),另外,在第二染色體亦發現一個叫做TIMELESS(簡稱TIM)。而後這三位學者針對兩個基因及其蛋白質產物,進行一連串實驗,結果揭開調控晝夜節律的分子機制,因此三位學者共同獲得1997年諾貝爾醫學獎。而後日本東京大學、神戶大學以及美國貝勒醫學院研究團隊,亦在小鼠和人類身上找到了PER和TIM基因的同源體,發現它們在視叉上核(suprachiasmatic nucleus, SCN)內特別活躍,這三位諾貝爾獎得主豐碩的研究成果,奠定「晝夜節律」的分子機制,也使與「晝夜節律」之相關研究有更突破性的發展。
截至目前為止,在此領域的相關學者均公認晝夜節律,是結合神經系統及分子調控的綜合體,有關分子調控方面,它是一種在細胞內自主而且自動回饋的迴路。它包括正向調節(positive regulator)及負向調節(negative regulator),造成一種互鎖的轉錄轉譯環(interlocked transcriptional translational feedback loop),從而形成一個在細胞內的自主節律器,可以啟動各式基因表現,包括新陳代謝、生物合成、訊號傳遞及細胞週期有關的基因。
包括人類在內的哺乳類,其主要管理晝夜節律基因包括BMAL1及CLOCK,在BMAL1及CLOCK之轉錄激活因子複合物,可以週期性啟動它的抑制因子,如:PERIOD(PER)及CRYPTOCHROME(CRY)等,另外還有一個迴路,正向調節的是RORα,負向調節的是REV-ERB。當BMAL1、CLOCK或RORα過多時(白天),則由PER、CRY及REV-ERBα取代(夜晚),在每天24小時輪流呈現,形成晝夜節律(圖三)。

晝夜節律失調,與癌症發生有關嗎? 當今科技和資訊發達的時代,由於物質文明的進步,人體與環境原本平衡的狀況,逐漸起了變化,生活步調也改變不少,有時因為夜間工作或娛樂造成作息大亂。有許多流行病學專家進行研究,發現從事夜間醫療工作者、空服員、24小時便利商店等相關女性工作者,得到乳癌的機率較高。亦有學者針對上下班時間不固定經常變動、作息紊亂的護理人員,進行多年的追蹤調查,結果發現,沒有正常作息的族群罹患乳癌的風險較高。
有些數據顯示罹癌風險可提高近40%。在中研院進行相關研究的黃雯華博士亦指出,晝夜節律(生理時鐘)如果是紊亂的話,確實會增加罹患乳癌的風險,若是已確診乳癌的病患,如果晝夜節律失調,則加速癌症的惡化。根據國內外的調查及統計發現,晝夜節律調控的基因,包括上述PER、CRY、CLOCK、BMAL、ROR及REV-ERB如果發生突變或缺失,再加上其他原有的致癌基因活化,抑癌基因被抑制,則很多種類的癌症發生率會增加(圖四)。

到目前為止,晝夜節律的紊亂或失調增加癌症的發生,已有很多學者研究,其原因歸納整理如下(圖五):

❶細胞週期變動及細胞凋亡機制失靈 在老鼠身上的細胞其晝夜節律週期如果PER基因改變的話,會導致癌症的發生。如果PER 基因功能消失,則可能引發惡性淋巴瘤。如果PER1及PER2正常的話,則細胞凋亡的機制會順利運作不至於產生癌症,包括大腸癌、乳癌及肺癌都有此現象。至於CRY基因對細胞週期及細胞凋亡機制亦有影響。
❷細胞新陳代謝之改變 晝夜節律亦會影響細胞之新陳代謝,如圖五所示,SIRT1及AMPK是細胞新陳代謝的調節者,當晝夜節律異常時會直接影響SIRT1及AMPK的訊息傳遞,導致能量的不平衡,甚至致癌。
❸異常晝夜節律易使癌細胞轉移,亦會使表皮癌細胞間質化,使惡性度增強,如胰臟癌BMAL1之表現降低,則惡性度增強。
在管腔型A的乳癌中,若PER及CRY之表現正常,其預後較佳。另外也有研究證實,PER之基因不正常表現,會增強癌細胞由表皮細胞間質化的現象,導致惡性度增加。
❹另外,在24小時晝夜節律當中,到晚上會釋放褪黑激素,如果節律失調,導致褪黑激素的釋放不理想,會使腫瘤加速成長。
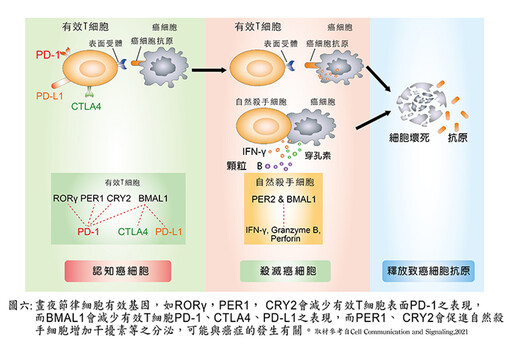
❺晝夜節律失調會使免疫功能降低,亦使癌症的發生率增加(圖六)。
如何調整晝夜節律使癌症的發生率降低?
根據華盛頓州立大學,轉譯醫學Yool Lee教授在去年(2021年)之綜述中特別提到,有些因素會使晝夜節律變差,像基因的缺陷(如節律基因的突變)或環境危險因子加劇(如長期熬夜、夜間工作、睡前大量攝食及經常長途旅行造成時差等)或人的老化、糖尿病、慢性病的影響,亦會破壞晝夜節律導致圖七右邊的癌症發生。
如果我們用心而且規律的訓練生理時鐘,例如晨起曬太陽、作息固定不熬夜、在晚上十點前就寢,使褪黑激素分泌正常,而使清晨的類固醇有足量釋放,加上飲食卡路里減少,間歇性斷食及規律運動,則可使晝夜節律之運作更加順暢,幫助每個細胞之生理功能表現正常(圖七)。

萬一得癌,化療用藥之給藥時間不同,會影響療效嗎?
最近Yool Lee教授在其綜述裡也特別提到因應晝夜節律進行時間療法(chronotherapy),在癌症醫學領域開始熱烈探討與進行,各類抗癌藥有其不同之作用機轉,其給藥時間可能要在不同的時段,到目前為止雖不完全成熟,但已有初步的成果呈現了,如圖八則闡述不同的化療藥物作用在細胞週期不同的階段,所以給藥的時間不一定要在同一時間,雖然比較麻煩,但對於人體正常組織的傷害會變小,而對癌組織的殺滅能力可以提升。
此種時間療法已有一些醫學中心正在進行臨床試驗(包括臨床一、二、三期均有),假以時日,可能有相當令人振奮的成果(圖八)。

結語
生活在地球上的我們,由於地球大約每24小時自轉一次,讓我們的生活有了晝夜之分;為了配合晝夜輪替的世界,我們的基因表現也需要「配合演出」,才能讓自己完美地生存在這個世界。人體共有超過兩萬五千個基因,這些基因當然不可能個別一一對晝夜環境變化進行反應,而是透過一般所謂的「時鐘基因組」(clock genes)來調節全身上下所有的基因表現。
2017年諾貝爾生理醫學獎頒給了美國的霍爾(Jeffrey C. Hall)、羅斯巴希(Michael Rosbash)和楊恩(Michael W. Young)對動物如何調節生理時鐘機制的研究,他們以果蠅(Drosophila melanogaster)為材料,發現果蠅的生理時鐘調節乃是透過包含PER(PERIOD)、TIM(TIMELESS)、DBT(DOUBLETIME)等幾個主要的基因來進行的。
現在也有越來越多的研究證實,連我們每日的心情和免疫系統也都跟身體內的晝夜節律有關,與癌症的發生亦有關係,本文特別將晝夜節律與癌症的關係,詳述如上,希望將來有關晝夜節律的研究或臨床試驗能更廣泛進行,使時間療法(Chronotherapy)在癌症醫學有其發展的空間。
本文摘自<常春月刊>476期
文:張金堅(乳癌防治基金會董事長)
由於從簡單的細菌到複雜的靈長類(包括人類),甚至植物,都有「晝夜節律」(circadian rhythm),又叫「約日節律」或「日變節律」,另外亦較常聽到的所謂「生理時鐘」(biologic clock)。在生醫學界中,通常以晝夜節律來描述一日之週期變化。Circa在拉丁的字首代表著「大約」、「大概」的意思,而diem(dian)在拉丁文的定義則是「一天」的意思,地球上的生物為什麼會出現晝夜節律現象呢?
基本而言,此等晝夜節律幫助地球上所有生物為白天的陽光和高溫,以及夜晚的黑暗和寒冷做好準備。好像含羞草白天張開葉子接受第一道陽光進行光合作用,晚上合起葉片一樣;羚羊在晨昏時出現在河邊,獅子就會在晨昏時前往水邊獲取獵物;在較於寒冷高緯度的動物需要在日落前找好棲身之地,才能躲過夜晚的寒冷。
這些案例證明了晝夜節律(生理時鐘)有其需要及功能存在,就好像正常人在一天24小時當中,因應日照、睡眠、休息、飲食、運動,其血壓、體溫及各類荷爾蒙也有週期性的起伏(圖一)。總之,從簡單的細菌、果蠅到複雜的靈長類,為什麼會有如此規則的節律呢?本文將由神經解剖及基因調控兩大方面來探討。

有關晝夜節律在神經解剖方面的相關探討
在1960年代,德國生理學家艾許夫博士(Jurgen Aschoff)將數名受試者個別關在沒有自然光的倉庫裡,發現即使在這樣的環境中,受試者仍保有大約24小時的睡醒週期(sleep-wake cycle),後來哈佛大學的柴斯勒(Chales Czeisler)及克諾勞爾(Richard E Kronauer)也發現同樣的現象。可見受試者的生理現象,並未受到人造環境的影響,不管是體溫、血壓或血液內各類激素濃度的變化,仍遵循24小時的規律。
直到1972年,芝加哥大學的摩爾博士(Robert Moore)及加州大學柏克萊分校的朱克教授(Irving Zucker)終於藉由腦損傷研究證實:人體體內的確有自行運作的生理時鐘,並證實調控晝夜節律的關鍵腦區就是在大腦下視丘(hypothalamus)中的視叉上核(suprachiasmatic nucleus,SCN),如SCN損傷,則無法表現正常的晝夜節律,在小鼠的試驗亦得到證實。
一般而言,當外界光線刺激可經由視神經,再經視網膜下視丘腦管道(retinohypothalamic tract, RHT)傳達到視叉上核(SCN),再影響到與晝夜節律有關的腦區,例如分泌褪黑激素的松果體(Pineal body),而後會有一系列的連續反應,因此視叉上核(SCN)被認為是最重要的中央生理時鐘,它主宰晝夜節律,會影響身體所有的器官、組織(如肝臟、胰臟、心臟、肺臟、血管、腎臟、淋巴系統及內分泌系統)等周邊的區域性生理時鐘,這些區域性的生理時鐘也會因為環境或各項生活因素,如天氣溫差變化、飲食、活動或休息等因素因應產生變化,並與中央生理時間同步協調(Synchronization),藉此調節各項生理功能,使身體維持在最佳的健康狀態。
如果熬夜、不規律生活、睡前大量攝食、沒有定期適當運動、長期夜班工作或飛行造成時差,都會使生理時鐘紊亂、交感神經活性上升、腎上腺素增加、胰島素阻抗性增加、導致血壓及血糖上升,同時有10種以上與發炎有關的介白素產生,免疫功能低下,易患心血管疾病、糖尿病,新陳代謝功能亦受影響,可能造成病態性肥胖,另外與精神有關的毛病,如:焦慮、憂鬱等,甚至造成記憶力減退,注意力不集中、失智等,最近研究發現與癌症亦有關聯(圖二)。

有關晝夜節律在分子控制方面的相關探討 有關於晝夜節律分子機制及基因研究,始自果蠅,由於果蠅體型小、生命週期短、繁殖快速,是進行此類研究的極佳模型,在1970年代,加州理工學院的科諾卡(Ron Konopka)和班瑟(Seymour Benzer)進行果蠅研究,利用誘變劑(mutagen),使果蠅發生基因突變,結果有兩種突變,一種小於正常24小時的短週期(19小時),及另一種大於24小時(28小時)的突變,後來由洛克斐勒大學的楊恩、布倫戴斯大學的霍爾(Jeffery Hall)和霍華休斯醫學中心的羅斯巴希(Michael Rosbash)相繼展開研究。
結果在1980年由楊恩及其團隊發現在X染色體有一基因突變命名為PERIOD(簡稱PER),另外,在第二染色體亦發現一個叫做TIMELESS(簡稱TIM)。而後這三位學者針對兩個基因及其蛋白質產物,進行一連串實驗,結果揭開調控晝夜節律的分子機制,因此三位學者共同獲得1997年諾貝爾醫學獎。而後日本東京大學、神戶大學以及美國貝勒醫學院研究團隊,亦在小鼠和人類身上找到了PER和TIM基因的同源體,發現它們在視叉上核(suprachiasmatic nucleus, SCN)內特別活躍,這三位諾貝爾獎得主豐碩的研究成果,奠定「晝夜節律」的分子機制,也使與「晝夜節律」之相關研究有更突破性的發展。
截至目前為止,在此領域的相關學者均公認晝夜節律,是結合神經系統及分子調控的綜合體,有關分子調控方面,它是一種在細胞內自主而且自動回饋的迴路。它包括正向調節(positive regulator)及負向調節(negative regulator),造成一種互鎖的轉錄轉譯環(interlocked transcriptional translational feedback loop),從而形成一個在細胞內的自主節律器,可以啟動各式基因表現,包括新陳代謝、生物合成、訊號傳遞及細胞週期有關的基因。
包括人類在內的哺乳類,其主要管理晝夜節律基因包括BMAL1及CLOCK,在BMAL1及CLOCK之轉錄激活因子複合物,可以週期性啟動它的抑制因子,如:PERIOD(PER)及CRYPTOCHROME(CRY)等,另外還有一個迴路,正向調節的是RORα,負向調節的是REV-ERB。當BMAL1、CLOCK或RORα過多時(白天),則由PER、CRY及REV-ERBα取代(夜晚),在每天24小時輪流呈現,形成晝夜節律(圖三)。

晝夜節律失調,與癌症發生有關嗎? 當今科技和資訊發達的時代,由於物質文明的進步,人體與環境原本平衡的狀況,逐漸起了變化,生活步調也改變不少,有時因為夜間工作或娛樂造成作息大亂。有許多流行病學專家進行研究,發現從事夜間醫療工作者、空服員、24小時便利商店等相關女性工作者,得到乳癌的機率較高。亦有學者針對上下班時間不固定經常變動、作息紊亂的護理人員,進行多年的追蹤調查,結果發現,沒有正常作息的族群罹患乳癌的風險較高。
有些數據顯示罹癌風險可提高近40%。在中研院進行相關研究的黃雯華博士亦指出,晝夜節律(生理時鐘)如果是紊亂的話,確實會增加罹患乳癌的風險,若是已確診乳癌的病患,如果晝夜節律失調,則加速癌症的惡化。根據國內外的調查及統計發現,晝夜節律調控的基因,包括上述PER、CRY、CLOCK、BMAL、ROR及REV-ERB如果發生突變或缺失,再加上其他原有的致癌基因活化,抑癌基因被抑制,則很多種類的癌症發生率會增加(圖四)。

到目前為止,晝夜節律的紊亂或失調增加癌症的發生,已有很多學者研究,其原因歸納整理如下(圖五):

❶細胞週期變動及細胞凋亡機制失靈 在老鼠身上的細胞其晝夜節律週期如果PER基因改變的話,會導致癌症的發生。如果PER 基因功能消失,則可能引發惡性淋巴瘤。如果PER1及PER2正常的話,則細胞凋亡的機制會順利運作不至於產生癌症,包括大腸癌、乳癌及肺癌都有此現象。至於CRY基因對細胞週期及細胞凋亡機制亦有影響。
❷細胞新陳代謝之改變 晝夜節律亦會影響細胞之新陳代謝,如圖五所示,SIRT1及AMPK是細胞新陳代謝的調節者,當晝夜節律異常時會直接影響SIRT1及AMPK的訊息傳遞,導致能量的不平衡,甚至致癌。
❸異常晝夜節律易使癌細胞轉移,亦會使表皮癌細胞間質化,使惡性度增強,如胰臟癌BMAL1之表現降低,則惡性度增強。
在管腔型A的乳癌中,若PER及CRY之表現正常,其預後較佳。另外也有研究證實,PER之基因不正常表現,會增強癌細胞由表皮細胞間質化的現象,導致惡性度增加。
❹另外,在24小時晝夜節律當中,到晚上會釋放褪黑激素,如果節律失調,導致褪黑激素的釋放不理想,會使腫瘤加速成長。
❺晝夜節律失調會使免疫功能降低,亦使癌症的發生率增加(圖六)。

如何調整晝夜節律使癌症的發生率降低?
根據華盛頓州立大學,轉譯醫學Yool Lee教授在去年(2021年)之綜述中特別提到,有些因素會使晝夜節律變差,像基因的缺陷(如節律基因的突變)或環境危險因子加劇(如長期熬夜、夜間工作、睡前大量攝食及經常長途旅行造成時差等)或人的老化、糖尿病、慢性病的影響,亦會破壞晝夜節律導致圖七右邊的癌症發生。
如果我們用心而且規律的訓練生理時鐘,例如晨起曬太陽、作息固定不熬夜、在晚上十點前就寢,使褪黑激素分泌正常,而使清晨的類固醇有足量釋放,加上飲食卡路里減少,間歇性斷食及規律運動,則可使晝夜節律之運作更加順暢,幫助每個細胞之生理功能表現正常(圖七)。

萬一得癌,化療用藥之給藥時間不同,會影響療效嗎?
最近Yool Lee教授在其綜述裡也特別提到因應晝夜節律進行時間療法(chronotherapy),在癌症醫學領域開始熱烈探討與進行,各類抗癌藥有其不同之作用機轉,其給藥時間可能要在不同的時段,到目前為止雖不完全成熟,但已有初步的成果呈現了,如圖八則闡述不同的化療藥物作用在細胞週期不同的階段,所以給藥的時間不一定要在同一時間,雖然比較麻煩,但對於人體正常組織的傷害會變小,而對癌組織的殺滅能力可以提升。
此種時間療法已有一些醫學中心正在進行臨床試驗(包括臨床一、二、三期均有),假以時日,可能有相當令人振奮的成果(圖八)。

結語
生活在地球上的我們,由於地球大約每24小時自轉一次,讓我們的生活有了晝夜之分;為了配合晝夜輪替的世界,我們的基因表現也需要「配合演出」,才能讓自己完美地生存在這個世界。人體共有超過兩萬五千個基因,這些基因當然不可能個別一一對晝夜環境變化進行反應,而是透過一般所謂的「時鐘基因組」(clock genes)來調節全身上下所有的基因表現。
2017年諾貝爾生理醫學獎頒給了美國的霍爾(Jeffrey C. Hall)、羅斯巴希(Michael Rosbash)和楊恩(Michael W. Young)對動物如何調節生理時鐘機制的研究,他們以果蠅(Drosophila melanogaster)為材料,發現果蠅的生理時鐘調節乃是透過包含PER(PERIOD)、TIM(TIMELESS)、DBT(DOUBLETIME)等幾個主要的基因來進行的。
現在也有越來越多的研究證實,連我們每日的心情和免疫系統也都跟身體內的晝夜節律有關,與癌症的發生亦有關係,本文特別將晝夜節律與癌症的關係,詳述如上,希望將來有關晝夜節律的研究或臨床試驗能更廣泛進行,使時間療法(Chronotherapy)在癌症醫學有其發展的空間。

