張金堅:揭開癌症幹細胞真面目
本文摘自《常春月刊》471期
文/張金堅(乳癌防治基金會董事長)
幹細胞(stem cell)定義為具有自我複製或更新(self-renewal)與分化為其他細胞能力(differentiation abilities)的細胞。例如胚胎幹細胞具有分化為各式細胞的能力(pluripotent);而成人身上的幹細胞,大多是各個組織或是器官的前驅細胞(progenitors),可以複製、分化為該譜系(lineage)的細胞,例如造血幹細胞(hematopoietic stem cell)可以分化為各種血球。
本文要探討的主題,癌症幹細胞(cancer stem cell,又叫腫瘤幹細胞),其理論基礎就是從體細胞的幹細胞理論發展而來。經過多年的發展,惡性腫瘤的癌症幹細胞理論已逐漸被大家接受,雖然惡性腫瘤起源與依賴一小群癌症幹細胞的細胞增殖的想法已經存在已久,但是在近年來,才因為生物科技的技術發展與進步,而有足夠的實驗數據加以證實癌症幹細胞存在的理論。
癌症幹細胞最早是由迪克(Dick)和他的同事在1994年,證明CD34+CD38-是急性骨髓性白血病(acute myeloid leukemia,AML)的癌症幹細胞,他們在依序的植入實驗中(serial transplantation),發現並且證明這一群細胞可以植入免疫缺陷小鼠並啟動白血病生成;而該群細胞只占數百萬AML細胞中的一小部分,這一部分也是生成腫瘤最原始的部分;除了血液腫瘤外,固態腫瘤在2003年,由克拉克(Clarke)和他的同事們,發現帶有標記CD44+CD24-/low的乳癌細胞,可以表現如急性骨髓性白血病之CD34+CD38-的癌症幹細胞相似的表現,也就是在連續數代小鼠移植實驗中,可以啟動乳癌腫瘤的生成,因此確立了CD44+CD24-/low為乳癌幹細胞。而後,各種癌症幹細胞的細胞表面標記逐一被找出來,確定了癌症幹細胞的理論。
癌症幹細胞的特性
傳統的癌症治療,是利用手術切除、化學治療、荷爾蒙治療或放射線治療,以抑制癌細胞的生長,進而引發其凋亡。但腫瘤具有異質性,會含有不同性質的癌細胞,大部分會因治療而被消滅。然而只有極少數惡性度高的癌細胞,經過化學藥物及放射線治療後仍可存活下來,並且躲過免疫系統的偵測,導致癌症在治療一段時間後出現復發或轉移情形(如圖一),
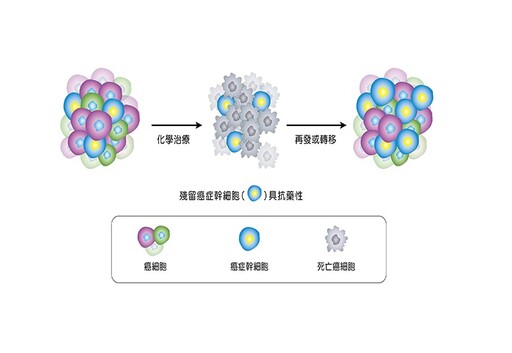
而且其復發或轉移部位的腫瘤,其癌細胞特性是由癌症幹細胞,藉由其對稱或不對稱的分裂而形成,其癌細胞的病理組織特性可能與原發病灶不盡相同,一般惡性度會增強(如圖二),此等癌細胞特叫癌症幹細胞,其具有下列特性:
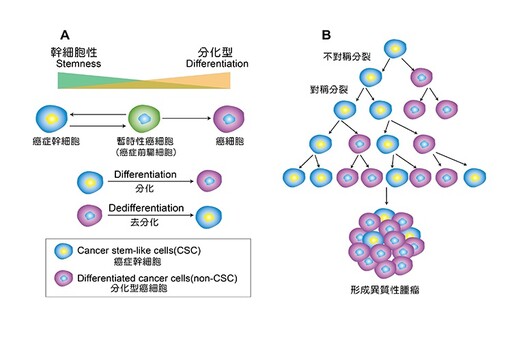
說明:
(A)其腫瘤內之細胞含癌症幹細胞、癌症前驅細胞與分化型的癌細胞,其所佔比例是動態的平衡,各類癌細胞隨時間變化,所佔比率不盡相同。
(B)癌症幹細胞會發生對稱及不對稱的分裂,造成異質性腫瘤。
❶癌症幹細胞具有較強DNA修復能力
癌症幹細胞可以依賴休眠狀態及生產更多具有活性的蛋白(如ATH-Chk2等)提升DNA修復能力抵抗治療,在DNA雙鏈斷裂時,細胞主要利用同源性重組(homologous recombination)或非同源性末端接合(non-homologous end joining,NHEJ)兩種修復方法。其原因乃是癌症幹細胞長期處於休眠、不分裂的狀態,有更多時間進行DNA修復。由於化療大多針對快速分裂的活躍細胞,這些癌症幹細胞便可逃過一劫;另外,休眠中的癌症幹細胞新陳代謝慢,本來積累的代謝物就較少,因此更能抵抗放射線治療的攻擊。
❷癌症幹細胞具有特殊的訊號傳遞路徑
癌症幹細胞的訊號傳遞,主要有Notch、Hedgehog和Wnt等三個癌症幹細胞常見的訊號傳遞路徑,例如肺癌幹細胞表現較高活性的Notch和Wnt的訊號,而大腸直腸癌則有Notch和Hedgehog等二個路徑,乳癌幹細胞則三個路徑均有,每一種癌症的傳遞路徑不盡相同,而且其活性度亦有強弱之分。激活這些途徑被認為是誘發腫瘤選殖(cloning)能力和促進腫瘤向外侵襲的原因之一。因此,這些幹細胞相關的路徑往往成為抗癌藥物發展的新標的,這類路徑的抑制劑,目前也相繼在各個臨床試驗研究進行中(如圖三之上半部)。
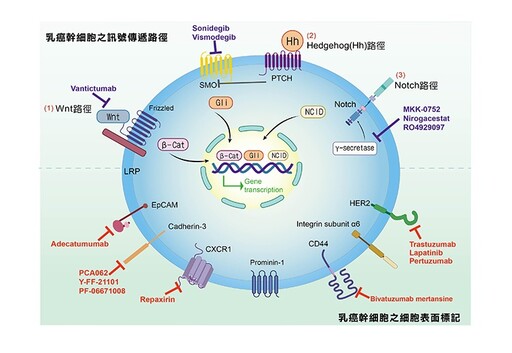
說明:
(A)本圖上半部是呈現乳癌幹細胞之訊號傳遞包括(1)Wnt、(2)Hedgehog及(3)Notch三大途徑,另外,圖中T表示目前正進行臨床試驗對抗此傳遞路徑的抑制藥物。
(B)本圖下半部是呈現乳癌幹細胞之表面生物標記,另外,圖中T表示目前在進行對抗表面生物標記之抑制劑之臨床試驗或已上市之藥物。
❸癌症幹細胞之表面有特殊之生物標記(Biomarker)
到目前為止,由於檢測技術的進步,國內外專家學者已利用流式細胞儀
(flow cytometery)分析各類癌症幹細胞之表面生物標記(如表一)。
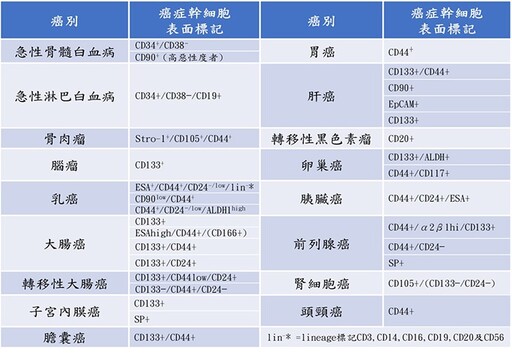
利用癌症幹細胞表面之特殊生物標記,研發對應之單株抗體或相關抑制藥物,可以抑制此等幹細胞的存活,也是目前臨床試驗之研發重點,如乳癌針對Her-2抑制之單株抗體已在乳癌病人身上使用(如圖三之下半部)。
❹癌症幹細胞與microRNA(miRNA)有關
最近研究顯示,某些微小核醣核酸microRNA(miR)例如miR-302 cluster,miR-372/373,let-7,與miR-200 family,可以調控其他基因的表現,影響細胞週期、上皮-間質轉化(epithelial-mesenchymal transition),進而與癌症幹細胞相關。Lin及其同事的研究顯示,miR-302會促進皮膚癌細胞的去分化,獲得幹細胞的特性。miR-200可以促使胰臟癌與大腸癌細胞,重新獲得癌症幹細胞的特性。由此可見,這些癌症幹細胞miRNA,經過標的基因與調控細胞週期,是參與癌症幹細胞形成的重要因素。
❺癌症幹細胞的微環境與去分化作用
一般癌症細胞也可以經由微環境的調控,重新獲取癌症幹細胞的特徵,若是腫瘤的微環境處於低氧狀態(hypoxia)之下,周遭的間質細胞、發炎細胞或是巨噬細胞可以分泌介白素6(Interleukin-6)等物質,經由前述的Hedgehog等相關訊號傳遞路徑,使細胞趨向於癌症幹細胞的特徵。另外,癌細胞也可以經過自分泌(autocrine)和旁分泌(paracrine)作用,來正向調控這些Notch、Hedgehog和Wnt等幹細胞的訊號路徑,使本來已經高度分化的癌細胞,反而會去分化(dedifferentiation),逆轉回原來癌症幹細胞的特性與作用(如圖四)。
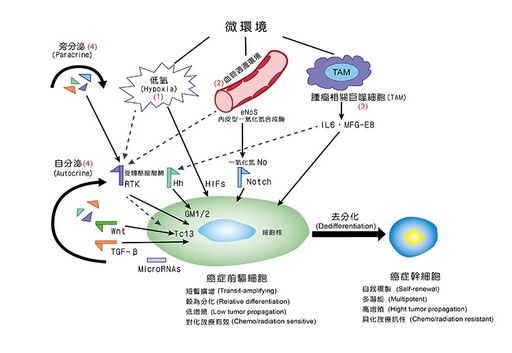
說明:
癌細胞(包括癌前驅細胞)可以因為微環境變化如:(1)缺氧、(2)癌細胞周圍血管變化、(3)腫瘤相關巨噬細胞或(4)癌細胞本身自分泌或旁分泌等之調控,使癌細胞發生去分化作用,而變成具有癌症幹細胞的特性。
❻癌症幹細胞具有抗藥性
癌症幹細胞有較多的抗凋亡分子(anti-apoptotic factors)、較高表現的藥物外排機能(drug efflux pumps),此現象在乳癌、大腸直腸癌或其他不同癌症都有發現,顯示這是各種癌症幹細胞的共同特點。當抗藥性產生時,腫瘤中之癌症幹細胞所佔的比例增加。如:惡性腦瘤中多形性膠質母細胞瘤(glioblastoma multiforme),在接受腦部放射線治療之後,CD133陽性的細胞比率反而上升,顯示腦瘤的幹細胞比率增加,雖腫瘤縮小了,但日後可能再發。另外,癌症幹細胞在癌的形成過程或造成復發轉移時,其所佔的比率是動態的,佔比可能起伏不定。
只針對癌症幹細胞的特異性標靶治療真的有效嗎?
如果只清除癌症幹細胞,這樣的治療足夠嗎?從目前動態的癌症幹細胞模型理論,我們可以看出,分化的癌細胞也同時需要治療,很明顯的,癌症幹細胞與其分化癌細胞,都需要進行有效的治療,才能將腫瘤一併消除。
針對外部環境訊號與細胞內的幹細胞訊號傳遞,直接給予標靶藥物抑制,是目前標靶藥物發展的一個想法,然而這在臨床病人應用上,可能是有問題的,因為正常的人體細胞也非常依賴於這些訊號傳遞路徑的;但是這些路徑在腫瘤可能被異常的活化,若給予適當的藥物或是合適劑量,來干擾這些異常活化訊號的傳遞,就可能可以提供一個有效的治療。例如,目前Notch抑制劑正在進行臨床試驗,評估用於治療結腸直腸癌的可行性。
臨床設計上,應該合併這一類藥物與其他傳統藥物針對非癌症幹細胞的部分(分化較佳的癌細胞),如此一來,才可以避免當癌症幹細胞比率下降之後,其他細胞經由去分化作用,獲得幹細胞的特徵與能力,造成腫瘤的復發。研究顯示肺癌的幹細胞可以藉由自分泌或是旁分泌作用活化與依賴c-KIT,若我們使用c-KIT的抑制劑加上肺癌的標準治療-白金類化學治療,則可以提高肺癌治療的成績。未來,這些類型的藥物陸續研發,必可提供治療癌症成功的契機,以改善病人的預後。當然,這些藥物必須通過嚴謹的臨床試驗,才能夠應用在病人身上(如圖三)。
癌症幹細胞面臨的問題尚待解決
癌症幹細胞是一個新興的領域,故仍有很多細節尚未明瞭;今後癌症幹細胞研究仍需著重解決下列幾個關鍵問題︰(1)癌症幹細胞特異性分子標記物不僅不同,而且表現強度亦各有不同,有待更精確的認定;(2)癌症幹細胞和其他癌細胞的相互作用與分子機轉仍有很多灰色地帶,有待釐清;(3)癌症幹細胞造成轉移之分子機制及惡性較低高度分化的癌細胞如何去分化,變成癌症幹細胞的機轉;(4)癌症幹細胞產生抗藥性機制這些都需要進一步驗證及闡述;此外針對癌症幹細胞的治療策略與其他療法合併使用亦有發展與改進的空間。
結語
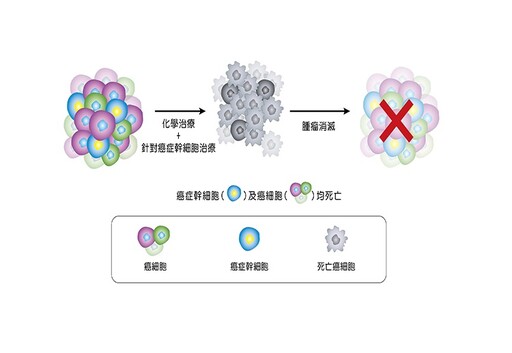
綜合上述討論,我們知道癌症幹細胞會受到許多因素有所改變,例如內在及外在環境的影響,而且呈現一個動態平衡。動態理論解釋了為什麼專門只針對癌症幹細胞的藥物,有可能不足以作為理想的抗癌策略,經常需要合併其他原有的傳統治療(包括化學、標靶、荷爾蒙及免疫治療等),方可以提升治療成效(如圖五)。
文/張金堅(乳癌防治基金會董事長)
幹細胞(stem cell)定義為具有自我複製或更新(self-renewal)與分化為其他細胞能力(differentiation abilities)的細胞。例如胚胎幹細胞具有分化為各式細胞的能力(pluripotent);而成人身上的幹細胞,大多是各個組織或是器官的前驅細胞(progenitors),可以複製、分化為該譜系(lineage)的細胞,例如造血幹細胞(hematopoietic stem cell)可以分化為各種血球。
本文要探討的主題,癌症幹細胞(cancer stem cell,又叫腫瘤幹細胞),其理論基礎就是從體細胞的幹細胞理論發展而來。經過多年的發展,惡性腫瘤的癌症幹細胞理論已逐漸被大家接受,雖然惡性腫瘤起源與依賴一小群癌症幹細胞的細胞增殖的想法已經存在已久,但是在近年來,才因為生物科技的技術發展與進步,而有足夠的實驗數據加以證實癌症幹細胞存在的理論。
癌症幹細胞最早是由迪克(Dick)和他的同事在1994年,證明CD34+CD38-是急性骨髓性白血病(acute myeloid leukemia,AML)的癌症幹細胞,他們在依序的植入實驗中(serial transplantation),發現並且證明這一群細胞可以植入免疫缺陷小鼠並啟動白血病生成;而該群細胞只占數百萬AML細胞中的一小部分,這一部分也是生成腫瘤最原始的部分;除了血液腫瘤外,固態腫瘤在2003年,由克拉克(Clarke)和他的同事們,發現帶有標記CD44+CD24-/low的乳癌細胞,可以表現如急性骨髓性白血病之CD34+CD38-的癌症幹細胞相似的表現,也就是在連續數代小鼠移植實驗中,可以啟動乳癌腫瘤的生成,因此確立了CD44+CD24-/low為乳癌幹細胞。而後,各種癌症幹細胞的細胞表面標記逐一被找出來,確定了癌症幹細胞的理論。
癌症幹細胞的特性
傳統的癌症治療,是利用手術切除、化學治療、荷爾蒙治療或放射線治療,以抑制癌細胞的生長,進而引發其凋亡。但腫瘤具有異質性,會含有不同性質的癌細胞,大部分會因治療而被消滅。然而只有極少數惡性度高的癌細胞,經過化學藥物及放射線治療後仍可存活下來,並且躲過免疫系統的偵測,導致癌症在治療一段時間後出現復發或轉移情形(如圖一),

而且其復發或轉移部位的腫瘤,其癌細胞特性是由癌症幹細胞,藉由其對稱或不對稱的分裂而形成,其癌細胞的病理組織特性可能與原發病灶不盡相同,一般惡性度會增強(如圖二),此等癌細胞特叫癌症幹細胞,其具有下列特性:

說明:
(A)其腫瘤內之細胞含癌症幹細胞、癌症前驅細胞與分化型的癌細胞,其所佔比例是動態的平衡,各類癌細胞隨時間變化,所佔比率不盡相同。
(B)癌症幹細胞會發生對稱及不對稱的分裂,造成異質性腫瘤。
❶癌症幹細胞具有較強DNA修復能力
癌症幹細胞可以依賴休眠狀態及生產更多具有活性的蛋白(如ATH-Chk2等)提升DNA修復能力抵抗治療,在DNA雙鏈斷裂時,細胞主要利用同源性重組(homologous recombination)或非同源性末端接合(non-homologous end joining,NHEJ)兩種修復方法。其原因乃是癌症幹細胞長期處於休眠、不分裂的狀態,有更多時間進行DNA修復。由於化療大多針對快速分裂的活躍細胞,這些癌症幹細胞便可逃過一劫;另外,休眠中的癌症幹細胞新陳代謝慢,本來積累的代謝物就較少,因此更能抵抗放射線治療的攻擊。
❷癌症幹細胞具有特殊的訊號傳遞路徑
癌症幹細胞的訊號傳遞,主要有Notch、Hedgehog和Wnt等三個癌症幹細胞常見的訊號傳遞路徑,例如肺癌幹細胞表現較高活性的Notch和Wnt的訊號,而大腸直腸癌則有Notch和Hedgehog等二個路徑,乳癌幹細胞則三個路徑均有,每一種癌症的傳遞路徑不盡相同,而且其活性度亦有強弱之分。激活這些途徑被認為是誘發腫瘤選殖(cloning)能力和促進腫瘤向外侵襲的原因之一。因此,這些幹細胞相關的路徑往往成為抗癌藥物發展的新標的,這類路徑的抑制劑,目前也相繼在各個臨床試驗研究進行中(如圖三之上半部)。

說明:
(A)本圖上半部是呈現乳癌幹細胞之訊號傳遞包括(1)Wnt、(2)Hedgehog及(3)Notch三大途徑,另外,圖中T表示目前正進行臨床試驗對抗此傳遞路徑的抑制藥物。
(B)本圖下半部是呈現乳癌幹細胞之表面生物標記,另外,圖中T表示目前在進行對抗表面生物標記之抑制劑之臨床試驗或已上市之藥物。
❸癌症幹細胞之表面有特殊之生物標記(Biomarker)
到目前為止,由於檢測技術的進步,國內外專家學者已利用流式細胞儀
(flow cytometery)分析各類癌症幹細胞之表面生物標記(如表一)。

利用癌症幹細胞表面之特殊生物標記,研發對應之單株抗體或相關抑制藥物,可以抑制此等幹細胞的存活,也是目前臨床試驗之研發重點,如乳癌針對Her-2抑制之單株抗體已在乳癌病人身上使用(如圖三之下半部)。
❹癌症幹細胞與microRNA(miRNA)有關
最近研究顯示,某些微小核醣核酸microRNA(miR)例如miR-302 cluster,miR-372/373,let-7,與miR-200 family,可以調控其他基因的表現,影響細胞週期、上皮-間質轉化(epithelial-mesenchymal transition),進而與癌症幹細胞相關。Lin及其同事的研究顯示,miR-302會促進皮膚癌細胞的去分化,獲得幹細胞的特性。miR-200可以促使胰臟癌與大腸癌細胞,重新獲得癌症幹細胞的特性。由此可見,這些癌症幹細胞miRNA,經過標的基因與調控細胞週期,是參與癌症幹細胞形成的重要因素。
❺癌症幹細胞的微環境與去分化作用
一般癌症細胞也可以經由微環境的調控,重新獲取癌症幹細胞的特徵,若是腫瘤的微環境處於低氧狀態(hypoxia)之下,周遭的間質細胞、發炎細胞或是巨噬細胞可以分泌介白素6(Interleukin-6)等物質,經由前述的Hedgehog等相關訊號傳遞路徑,使細胞趨向於癌症幹細胞的特徵。另外,癌細胞也可以經過自分泌(autocrine)和旁分泌(paracrine)作用,來正向調控這些Notch、Hedgehog和Wnt等幹細胞的訊號路徑,使本來已經高度分化的癌細胞,反而會去分化(dedifferentiation),逆轉回原來癌症幹細胞的特性與作用(如圖四)。

說明:
癌細胞(包括癌前驅細胞)可以因為微環境變化如:(1)缺氧、(2)癌細胞周圍血管變化、(3)腫瘤相關巨噬細胞或(4)癌細胞本身自分泌或旁分泌等之調控,使癌細胞發生去分化作用,而變成具有癌症幹細胞的特性。
❻癌症幹細胞具有抗藥性
癌症幹細胞有較多的抗凋亡分子(anti-apoptotic factors)、較高表現的藥物外排機能(drug efflux pumps),此現象在乳癌、大腸直腸癌或其他不同癌症都有發現,顯示這是各種癌症幹細胞的共同特點。當抗藥性產生時,腫瘤中之癌症幹細胞所佔的比例增加。如:惡性腦瘤中多形性膠質母細胞瘤(glioblastoma multiforme),在接受腦部放射線治療之後,CD133陽性的細胞比率反而上升,顯示腦瘤的幹細胞比率增加,雖腫瘤縮小了,但日後可能再發。另外,癌症幹細胞在癌的形成過程或造成復發轉移時,其所佔的比率是動態的,佔比可能起伏不定。
只針對癌症幹細胞的特異性標靶治療真的有效嗎?
如果只清除癌症幹細胞,這樣的治療足夠嗎?從目前動態的癌症幹細胞模型理論,我們可以看出,分化的癌細胞也同時需要治療,很明顯的,癌症幹細胞與其分化癌細胞,都需要進行有效的治療,才能將腫瘤一併消除。
針對外部環境訊號與細胞內的幹細胞訊號傳遞,直接給予標靶藥物抑制,是目前標靶藥物發展的一個想法,然而這在臨床病人應用上,可能是有問題的,因為正常的人體細胞也非常依賴於這些訊號傳遞路徑的;但是這些路徑在腫瘤可能被異常的活化,若給予適當的藥物或是合適劑量,來干擾這些異常活化訊號的傳遞,就可能可以提供一個有效的治療。例如,目前Notch抑制劑正在進行臨床試驗,評估用於治療結腸直腸癌的可行性。
臨床設計上,應該合併這一類藥物與其他傳統藥物針對非癌症幹細胞的部分(分化較佳的癌細胞),如此一來,才可以避免當癌症幹細胞比率下降之後,其他細胞經由去分化作用,獲得幹細胞的特徵與能力,造成腫瘤的復發。研究顯示肺癌的幹細胞可以藉由自分泌或是旁分泌作用活化與依賴c-KIT,若我們使用c-KIT的抑制劑加上肺癌的標準治療-白金類化學治療,則可以提高肺癌治療的成績。未來,這些類型的藥物陸續研發,必可提供治療癌症成功的契機,以改善病人的預後。當然,這些藥物必須通過嚴謹的臨床試驗,才能夠應用在病人身上(如圖三)。
癌症幹細胞面臨的問題尚待解決
癌症幹細胞是一個新興的領域,故仍有很多細節尚未明瞭;今後癌症幹細胞研究仍需著重解決下列幾個關鍵問題︰(1)癌症幹細胞特異性分子標記物不僅不同,而且表現強度亦各有不同,有待更精確的認定;(2)癌症幹細胞和其他癌細胞的相互作用與分子機轉仍有很多灰色地帶,有待釐清;(3)癌症幹細胞造成轉移之分子機制及惡性較低高度分化的癌細胞如何去分化,變成癌症幹細胞的機轉;(4)癌症幹細胞產生抗藥性機制這些都需要進一步驗證及闡述;此外針對癌症幹細胞的治療策略與其他療法合併使用亦有發展與改進的空間。
結語
綜合上述討論,我們知道癌症幹細胞會受到許多因素有所改變,例如內在及外在環境的影響,而且呈現一個動態平衡。動態理論解釋了為什麼專門只針對癌症幹細胞的藥物,有可能不足以作為理想的抗癌策略,經常需要合併其他原有的傳統治療(包括化學、標靶、荷爾蒙及免疫治療等),方可以提升治療成效(如圖五)。


